Abstract
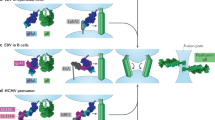
Enveloped viruses enter cells by fusion between viral and cellular membranes which is catalyzed by specialized fusogenic glycoproteins (g) on the viral surface. Many viruses use a single fusion protein for entry. In contrast, herpesviruses depend on a complex fusion machinery. Here, we discuss the role of the individual herpesvirus fusion machinery components and answer two basic questions: why does the herpesvirus fusion protein gB depend on other glycoproteins for fusion, and can gB be transformed to function autonomously?
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Rey FA, Lok SM (2018) Common features of enveloped viruses and implications for immunogen design for next-generation vaccines. Cell 172: 1319–1334
Vallbracht M, Backovic M, Klupp BG et al. (2019) Common characteristics and unique features: a comparison of the fusion machinery of the alphaherpesviruses pseudorabies virus and herpes simplex virus. Adv Virus Res 104: 225–281
Vallbracht M, Brun D, Tassinari M et al. (2018) Structure-function dissection of pseudorabies virus glycoprotein B fusion loops. J Virol 92: e01203–17
Heldwein EE, Lou H, Bender FC et al. (2006) Crystal structure of glycoprotein B from herpes simplex virus 1. Science 313: 217–220
Backovic M Jardetzky TS (2009) Class III viral membrane fusion proteins. Curr Opin Struct Biol 19:189–196
Klupp BG, Mettenleiter TC (1999) Glycoprotein gL-inde-pendent infectivity of pseudorabies virus is mediated by a gD-gH fusion protein. J Virol 73: 3014–3022
Schmidt J, Gerdts V, Beyer J et al. (2001) Glycoprotein D-independent infectivity of pseudorabies virus results in an alteration of in vivo host range and correlates with mutations in glycoproteins B and H. J Virol 75: 10054–10064
Schröter C, Vallbracht M, Altenschmidt J et al. (2015) Mutations in pseudorabies virus glycoproteins gB, gD, and gH functionally compensate for the absence of gL. J Virol 90: 2264–2272
Vollmer B, Prazak V, Vasishtan D et al. (2020) The prefusion structure of herpes simplex virus glycoprotein B. Sci Adv 6: eabc1726
Nixdorf R, Klupp BG, Mettenleiter TC (2001) Restoration of function of carboxy-terminally truncated pseudorabies virus glycoprotein B by point mutations in the ectodomain. J Virol 75: 11526–11533
Vallbracht M, Lötzsch H, Klupp BG et al. (2021) In vitro viral evolution identifies a critical residue in the alphaherpes-virus fusion glycoprotein B ectodomain that controls gH/gL-independent entry. mBio 12: e00557–21
Funding
Funding note: Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Wir danken Walter Fuchs, Felix A. Rey, Marija Backovic, Kay Grünewald und Benjamin Vollmer für die exzellente und freundschaftliche Zusammenarbeit. Besonders danken wir der Deutschen Forschungsgemeinschaft für die essenzielle Förderung.
Melina Vallbracht, Barbara G. Klupp und Thomas C. Mettenleiter (v. l. n. r.)
Melina Vallbracht 2009–2015 Studium der Biowissenschaften an der Universität Münster. 2015–2018 Promotion und 2018–2021 Postdoktorandin am Institut für Molekulare Virologie und Zellbiologie (IMVZ) am Friedrich-Loeffler-Institut (FLI), Insel Riems. Seit 2021 Postdoktorandin am Zentrum für Infektiologie-Virologie, Universitätsklinikum Heidelberg.
Barbara G. Klupp 1982–1988 Biologiestudium an der Universität Tübingen. 1989–1992 Promotion und 1992–1994 Postdoktorandin an der Bundesforschungsanstalt für Viruskrankheiten der Tiere in Tübingen (BFAV, heute: FLI). Seit 1994 Arbeitsgruppenleiterin am IMVZ, FLI, Insel Riems und seit 2020 stellvertretende (kommissarisch) Leiterin des Instituts.
Thomas C. Mettenleiter 1977–1982 Biologiestudium an der Universität Tübingen. 1982 Beginn der Arbeiten an der Bundesforschungsanstalt für Viruskrankheiten der Tiere (BFAV, heute: FLI). 1985 Promotion. 1986–1987 Postdoktorand am Department of Microbiology, Medical School, Vanderbilt University, Nashville, USA. 1991 Habilitation in Tübingen. 1994–2020 Leiter des IMVZ, seit 1997 Präsident des FLI.
Rights and permissions
Open Access: Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Vallbracht, M., Klupp, B.G. & Mettenleiter, T.C. Die komplexe Fusionsmaschinerie der Herpesviren. Biospektrum 28, 168–170 (2022). https://doi.org/10.1007/s12268-022-1718-5
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-022-1718-5